Halo Sobat100, It's Science Time. Kembali tim100 menyapa kalian semua dalam kabar sains. Tahukah kalian?? Bahwa 3 hari di awal minggu ini 2-4 Oktober 2017 telah diumumkan para peraih Hadiah Nobel tahun 2017 di bidang Sains. Siapa sajakah mereka? Apa saja yang ditemukan?
Penasaran?
Silakan simak penjelasan berikut ini.
1. Bidang Fisiologi
Hadiah Nobel tahun 2017 dalam Fisiologi atau Medis diberikan kepada Jeffrey C. Hall, Michael Rosbash dan Michael W. Young atas penemuan mekanisme molekuler yang mengendalikan ritme sirkadian. Irama sirkadian didorong oleh jam biologis internal yang mengantisipasi siklus siang / malam untuk mengoptimalkan fisiologi dan perilaku organisme.

Kiri : Jeffrey C. Hall (lahir 3 May 1945), Tengah : Michael Rosbash (lahir 7 Maret 1944), Kanan : Michael W. Young (lahir 28 Maret 1949)
Latar Belakang
Pengamatan bahwa organisme menyesuaikan fisiologi dan perilaku mereka hingga waktu dalam mode sirkadian telah didokumentasikan untuk waktu yang lama, namun keberadaan jam sirkuler endogen akhirnya akan terbentuk sampai abad ke-20. Pada tahun 1971, Seymour Benzer dan Ronald Konopka mengidentifikasi mutan lalat buah Drosophila yang menunjukkan perubahan pada siklus normal 24 jam dari eklositas pupal dan aktivitas lokomotor. Percobaan menunjukkan bahwa mutasi melibatkan gen yang sama (yang kemudian diberi nama). Satu dekade kemudian, Hall dan Rosbash, berkolaborasi di Brandeis University, dan Young, di Universitas Rockefeller, mengisolasi dan secara molekuler mengkarakterisasi periode gen tersebut. Namun, struktur dan urutannya tidak segera menyarankan mekanisme molekuler untuk jam sirkadian. Serangkaian terobosan, termasuk identifikasi gen lain yang bermitra dengan periode, dari Hall, Rosbash dan Young akhirnya mengarah pada gagasan Transcription - Translation Feedback Loop (TTFL). Dalam mekanisme ini, transkripsi periode dan gen mitranya yang abadi ditekan oleh produk gen mereka sendiri - protein PERIOD (PER) dan TIME - LESS (TIM), menghasilkan osilasi otonom. Pada saat itu, mekanisme transkripsi tidak jelas, dan penemuan TTFL sirkadian mandiri adalah paradigma baru.
Studi lebih lanjut mengungkapkan serangkaian loop umpan balik translasi transkripsi saling terkait, bersama dengan jaringan reaksi yang kompleks. Ini melibatkan protein yang terdistribusi fosforilasi dan degradasi komponen TTFL, asembli kompleks protein, translokasi nuklir dan modifikasi pasca translasi lainnya, menghasilkan osilasi dengan jangka waktu ~ 24 jam. Osilator sirkadian dalam sel individu merespons secara berbeda terhadap sinyal entraining dan mengendalikan berbagai keluaran fisiologis, seperti pola tidur, suhu tubuh, pelepasan hormon, tekanan darah, dan metabolisme. Penemuan seminal oleh Hall, Rosbash dan Young mengungkapkan mekanisme fisiologis penting yang menjelaskan adaptasi sirkadian, dengan implikasi penting bagi kesehatan dan penyakit manusia.
Fitur utama kehidupan di Bumi adalah kemampuan untuk beradaptasi dengan lingkungan. Lokasi geografis yang berbeda memiliki lingkungan dan organisme yang berbeda sesuai dengan kondisi lazim yang ada di lokasi mereka untuk meningkatkan kelangsungan hidup mereka. Namun, pada lokasi tertentu, perubahan lingkungan dan suhu lingkungan terjadi setiap hari sebagai konsekuensi dari rotasi bumi pada porosnya. Untuk menyesuaikan diri terhadap perubahan tersebut, sebagian besar organisme telah mengembangkan jam biologis internal yang mengantisipasi siklus siang / malam dan membantu mereka mengoptimalkan fisiologi dan perilaku mereka. Ritme harian internal ini dikenal sebagai "sirkadian", dari kata Latin circa berarti "sekitar" dan dies artinya "hari". Ritme sirkadian kuno dan dilestarikan sepanjang evolusi. Mereka diketahui ada dalam bentuk kehidupan dari cyanobacteria uniseluler dan protozoa semua organisme multiseluler, termasuk jamur, tumbuhan, serangga, hewan pengerat dan manusia. Blok bangunan sistem sirkadian terdiri dari generator irama 24 jam mandiri atau osilator, pengaturan atau mekanisme entraining yang menghubungkan osilator internal dengan rangsangan eksternal (disebut sebagai zeitgebers, yaitu pencatat waktu), seperti mekanisme cahaya dan output untuk memungkinkan penjadwalan tepat waktu proses fisiologis
Dari irama sampai jam
Pengamatan bahwa organisme menyesuaikan fisiologi dan perilaku mereka hingga waktu dalam mode sirkadian telah didokumentasikan untuk waktu yang lama dan umumnya disepakati untuk memulai dengan pengamatan gerakan daun dan bunga pada tanaman. Misalnya, daun mimosa tanaman tutup pada malam hari dan buka di siang hari. Pada tahun 1729, astronom Prancis Jean Jacques d'Ortous de Mairan menempatkan tanaman mimosa dalam kegelapan dan mengamati bahwa dedaunan tetap terbuka dan tertutup secara berirama pada waktu yang tepat hari itu, menunjukkan asal mula ritme harian yang endogen (Gambar 1). Sekitar dua ratus tahun kemudian, ahli fisiologi tumbuhan Jerman dan pelopor penelitian ritme sirkadian, Erwing Bünning, dengan susah payah menghubungkan daun tanaman kacang ke kimograf dan mencatat pergerakan daun pada siklus siang hari / malam yang normal dan dalam kondisi cahaya konstan.
Ia mengamati bahwa irama gerakan daun tetap bertahan. Pertanyaan apakah perilaku sirkadian pada tumbuhan dan hewan diperintah oleh jam endogen, atau hanya merupakan reaksi terhadap rangsangan eksternal yang bersifat sirkadian, akan diperdebatkan dengan hangat selama beberapa dekade. Akhirnya, keberadaan jam sirkuler endogen akan terjadi dan menjadi mapan sampai abad ke-20.
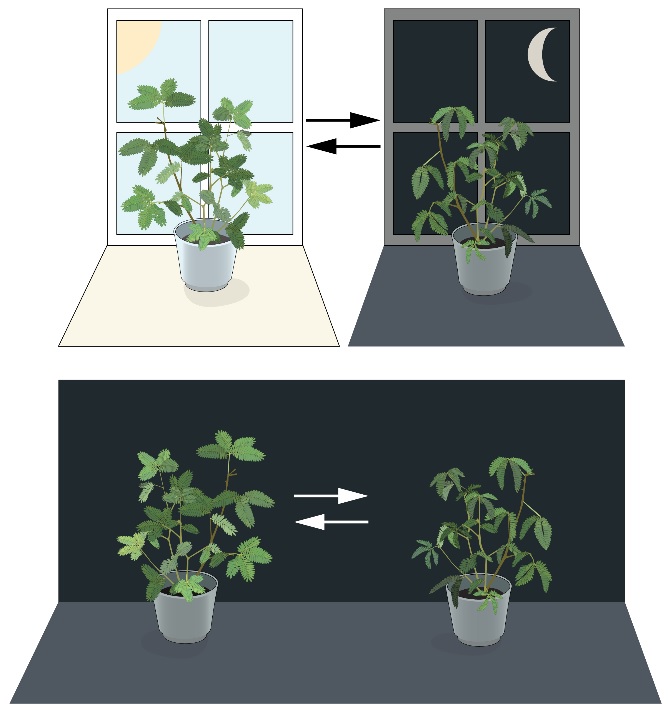
Gambar 1. Jam biologis internal.
Daun tanaman mimosa terbuka ke arah matahari pada siang hari dan menjelang senja. Jean Jacques d'Ortous de Mairan menempatkan tanaman mimosa dalam kegelapan yang konstan dan menemukan bahwa daun terus mengikuti ritme harian mereka selama beberapa hari. Ini menunjukkan bahwa Tanaman mimosa memiliki jam otonom sel yang bisa menjaga ritme biologis meski dalam kondisi konstan.
Heritabilitas ritme sirkadian dan gen jam
Seiring waktu, banyak sifat fisiologis yang relevan selain gerakan daun periodik yang ditemukan dikendalikan oleh jam fisiologis dan pewarisan ritme sirkadian mulai dianggap sebagai produk seleksi alam. Studi klasik Erwing Bünning pada tahun 1930 menunjukkan bahwa irama sirkadian pada tanaman dapat diwariskan meskipun tanaman induk terpapar pada periode cahaya non-sirkadian dan bahwa persilangan antara cabang dengan periode yang bervariasi menghasilkan tanaman dengan periode intermediet. Pada pertengahan 1960-an, sebuah komunitas peneliti chronobiology yang menyelidiki jam biologis telah mapan dan konsep gen jam mulai dipertimbangkan.
Pada sekitar waktu inilah Seymour Benzer dan muridnya Ronald Konopka, yang bekerja di Institut Teknologi California, memulai penelitian untuk mengidentifikasi lalat buah mutan dengan perubahan fenotip sirkadian. Tidak seperti beberapa ilmuwan genetika dan perilaku saat itu, Benzer dengan tegas percaya bahwa perilaku spesifik dapat dipengaruhi oleh tindakan gen tunggal dan bahwa adalah mungkin untuk menunjukkan hal ini dengan mengisolasi organisme dengan perilaku yang berubah yang membawa mutasi pada gen individual. Dengan menggunakan strategi mutagenesis berbasis kimia klasik, Benzer dan Konopka mengisolasi tiga strain yang berbeda lalat mutan yang menunjukkan perubahan pada siklus normal 24 jam eklositas pupal dan aktivitas lokomotor[1].
Satu mutan ternyata aritmik, yang lain memiliki periode yang lebih pendek yaitu 19 jam, dan yang ketiga memiliki yang lebih lama yaitu periode 28 jam. Percobaan pemetaan, dengan menggunakan penanda genetik yang diketahui pada saat itu, secara kasar melokalisasi ketiga mutan tersebut ke daerah kromosom X yang sama dengan lalat buah. Yang penting, tes pelengkap menyarankan agar ketiga mutasi tersebut melibatkan gen yang sama, yang kemudian diberi nama periode. Berdasarkan hal tersebut, Benzer dan Konopka memprediksikan bahwa mutan yang aritmik akan membawa mutasi omong kosong yang menginaktivasi gen tersebut, dan bahwa mutan dengan periode lebih lama dan lebih pendek akan membawa mutasi missense yang mengubah fungsi produk gen dengan cara yang berlawanan. Nanti hasil kerja menunjukkan kedua prediksi itu benar. Meski Benzer akan beralih ke topik lain, Konopka terus mengerjakan lokus periode, pemetaan posisi kromosom dengan presisi lebih tinggi. Namun, gen periode tidak akan secara molekuler dikloning dan diurutkan sampai pertengahan 1980an melalui karya Jeffrey Hall dan Michael Rosbash, berkolaborasi di Universitas Brandeis, dan Michael Young, di Rockefeller University.[2][3][4][5] Gen jam pertama diisolasi dan strukturnya dicirikan secara molekuler. Namun, baik identifikasi genetik asli periode maupun kloning dan sekuensing cDNA-nya menunjuk pada mekanisme molekuler untuk jam sirkadian.
Transcription-Translation Feedback Loop
Pada tahun-tahun setelah kloning periode, beberapa model diusulkan untuk menjelaskan bagaimana produk protein PER mungkin berfungsi untuk menghasilkan osilasi sirkadian. Model "membran gradient" diusulkan di mana PER dibayangkan berfungsi seperti pompa untuk membangun gradien melintasi membran yang, setelah mencapai ambang batas, akan hilang melalui saluran yang peka cahaya. Dalam model lain, protein PER diusulkan menjadi proteoglikan yang membawa sel bersama, sehingga memudahkan pembentukan koneksi antar sel melalui persimpangan celah. Serangkaian terobosan akhirnya dimungkinkan dengan tersedianya antibodi PER yang andal. Pertama adalah penemuan dari laboratorium Hall dan Rosbash dari siklus 24 jam dengan kelimpahan protein PER pada neuron otak terbang, dengan puncak pada malam hari.[6]
MRNA yang dikodekan oleh gen periode juga menunjukkan kelimpahan siklus sirkadian pada fly brain, menunjukkan bahwa siklus protein PER dihasilkan dari siklus mRNA periode. Menariknya, puncak tingkat mRNA periode terjadi di awal malam, beberapa jam sebelum puncak kelimpahan protein PER.[7] Yang penting, mutan omong kosong tidak mampu menghasilkan tingkat mRNA periode, namun protein PER tipe liar dapat menyelamatkan ekspresi mRNA siklik. Berdasarkan pengamatan ini, model umpan balik autoregulator negatif lahir, di mana akumulasi protein PER menghasilkan redaman ekspresi mRNA periode.[7] Selanjutnya, protein PER ditemukan sebagai protein nuklir dan penghubung antara inti sel dan sitoplasma dengan cara yang diatur secara temporer, memberikan dukungan untuk gagasan bahwa protein PER adalah pengatur transkripsi dari beberapa jenis.[8] Dengan pemahaman yang baru, Young menemukan timeless, gen tambahan yang mempengaruhi jam sirkadian.[9][10] Dalam serangkaian penemuan berikutnya, laboratorium Young menemukan bahwa tingkat mRNA timeless juga diawetkan dengan periode 24 jam, dan bahwa TIM dapat mengikat secara langsung ke PER, yang mempengaruhi lokalisasi dan kelimpahan nuklirnya dengan menghalangi degradasi PER.[11][12][13] Yang penting, siklus ekspresi periode dihapuskan pada lalat mutan timeless dan, sebaliknya, siklus sirkadian dalam ekspresi timeless hilang pada lalat mutan periode.[10][12] Kemajuan ini mengkonsolidasikan kerangka konseptual dasar TTFL sebagai mekanisme untuk mempromosikan siklus sirkadian dalam autoregulasi gen jam (Gambar 2A). Pada saat itu, mekanisme transkripsi tidak jelas dan, seperti disebutkan di atas, berbagai alternatif dipertimbangkan. Dengan demikian, penemuan TTFL sirkadian mandiri merupakan paradigma baru.
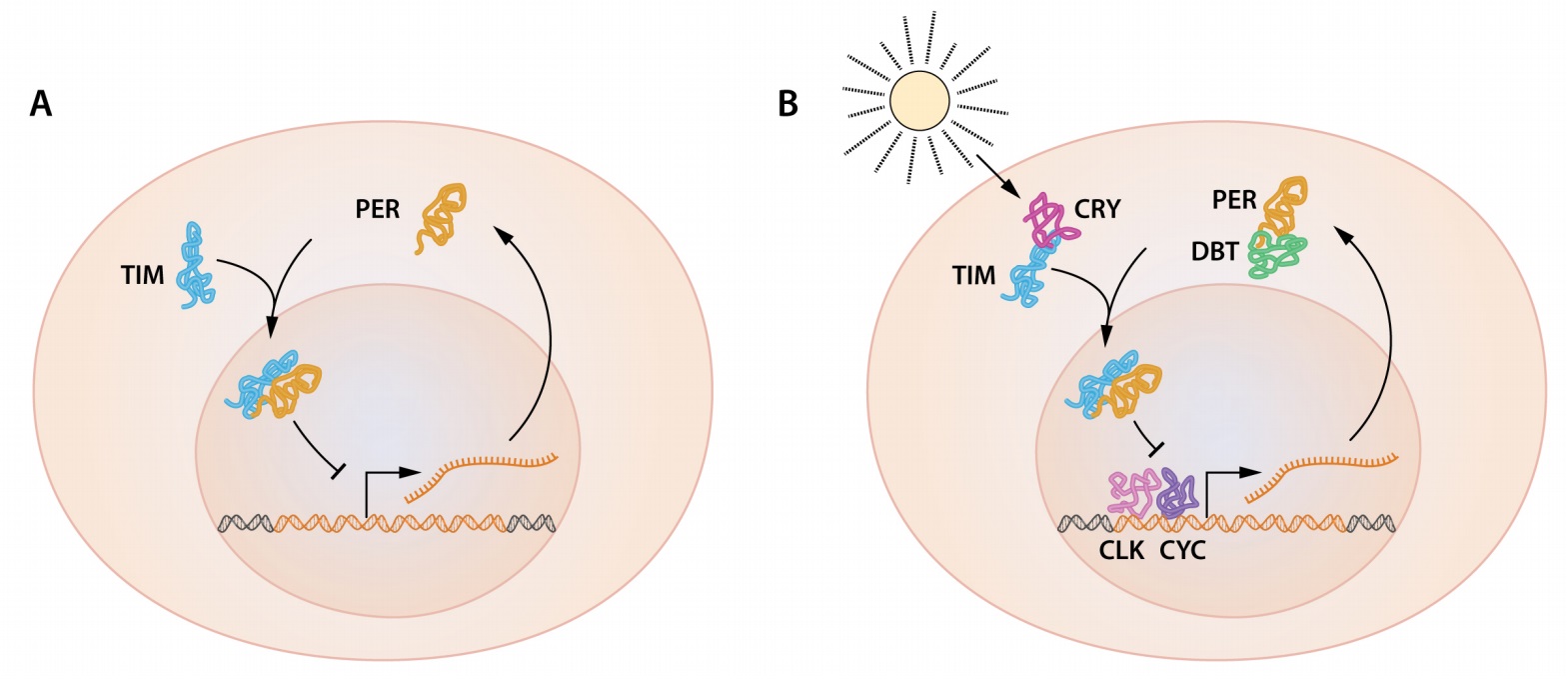
Gambar 2. Sebuah ilustrasi yang disederhanakan dari regulasi umpan balik dari gen periode.
A) Kedua periode mRNA dan protein PER berosilasi, dengan protein PER mengumpulkan beberapa jam setelah puncak pada periode mRNA. PER protein terlokalisasi di dalam nukleus, dan aktivitas gen periode berosilasi sebagai akibat dari inhibisi umpan balik protein PI dari gennya sendiri.
B) Protein tambahan sangat penting untuk osilasi gen periode. Protein TIM, yang dikodekan oleh gen abadi juga berosilasi dan berinteraksi dengan protein PER. Interaksi sangat penting untuk akumulasi protein PER dan penindakan gen periode. Protein DBT dikodekan oleh gen doubletime. DBT adalah protein kinase yang memfosforilasi PER, yang menyebabkan degradasi protein PER. Degradasi protein PER yang diperantarai DBT berkontribusi terhadap penundaan antara periode mRNA dan akumulasi protein PER. CLK dan CYK, yang dikodekan oleh gen jam dan siklus, adalah dua faktor transkripsi yang mengaktifkan gen periode.
Mekanisme di mana transkripsi periodik dan waktu tidak aktif tidak diketahui. Pertanyaan ini diselesaikan dengan penemuan gen jam dan siklus.[14][15] (Gen jam pertama kali diidentifikasi pada tikus, oleh Joseph Takahashi[16] Produk gen, CLOCK (CLK) dan CYCLE (CYC) berinteraksi satu sama lain, mengandung motif heliks-loop-helix (bHLH) dasar, dan mengikat elemen tertentu dalam periode dan gen timeless, sehingga secara positif mengatur transkripsi mereka. Studi selanjutnya akan menunjukkan bahwa TIM dan PER bertindak sebagai regulator negatif aktivitas CLK, dan dengan ini, loop umpan sirkadian ditutup.[17]
Penelitian terbaru memodelkan jam kerja sirkadian sangat kompleks dan mencakup banyak komponen tambahan yang secara kolektif berkontribusi terhadap ketahanan dan periodisitas sirkadiannya.[18] Yang penting, karena reaksi transkripsi dan translasi biasanya cepat, penundaan yang substansial harus diterapkan pada mekanisme TTFL inti untuk menghasilkan osilasi 24 jam. Hal ini dicapai dengan jaringan reaksi yang kompleks yang melibatkan protein fosforilasi dan degradasi komponen TTFL, asembli kompleks protein, translokasi nuklir dan modifikasi pasca translasi lainnya.[18] Pengamatan kunci yang menunjukkan mekanisme yang mendasari penundaan tersebut berasal dari penemuan Young dari gen doubletime, yang mengkodekan sebuah kinase. DOUBLETIME (DBT) yang memfosforilasi PER dan meningkatkan degradasinya.[19] Protein tambahan mengintegrasikan masukan lingkungan yang bisa mempengaruhi jam (Gambar 2B). Misalnya, cahaya dapat mengaktifkan produk protein dari gen cryptochrome cry (CRY) dan mempromosikan ikatannya ke TIM, menyebabkan degradasi pada proteasom.[20][21] Saat pagi tiba, TIM terdegradasi, meninggalkan PER rentan terhadap fosforilasi oleh DBT dan degradasi berikutnya.
Jam sirkadian pada organisme lain
Mekanisme TTFL juga merupakan prinsip dasar jam sirkadian pada organisme multiselular lainnya, termasuk manusia. Beberapa homolog protein jam inti di Drosophila, termasuk CLK dan PER, memainkan peran serupa dalam ketepatan waktu sirkadian mamalia.[22] Meskipun tanaman terutama pengguna faktor transkripsi yang tidak homolog dengan jam sirkadian Drosophila, TTFL adalah prinsip utama pemersatu.[23] Namun, dalam cyanobacteria, jenis osilator sirkadian independen yang berbeda telah dijelaskan bergantung pada kejadian fosforilasi protein sekuensial.[24] Hebatnya, irama sirkadian dapat dilarutkan secara in vitro menggunakan protein jam cyanobacteria yang dimurnikan dan ATP.[25] Sebuah osilasi transkripsi-independen yang dihasilkan dari hipoksidasi peroksiredoksin juga telah dijelaskan dalam eukariota, termasuk pada eritrosit manusia.[26][27] Relevansi fisiologis dari osilasi TTFL independen tidak diketahui. Namun demikian, hasil ini menunjukkan bahwa mekanisme tambahan untuk menghasilkan osilasi sirkadian juga ada pada sel mamalia.
Pengaturan dan sinkronisasi jam biologis
Program sirkadian diatur pada tingkat pusat dan perifer. Pada mamalia, alat pacu jantung pusat terletak di inti suprachiasmatik (SCN) hipotalamus dan berfungsi sebagai pusat jam sirkadian. Retina menerima masukan fotik dan mengirimkan informasi ini ke SCN, yang mensinkronisasi jam seluler neuronalnya sendiri. Jam utama mengatur ritme sirkadian di seluruh tubuh melalui faktor humoral dan sistem saraf otonom perifer. Namun, kapasitas ekspresi gen sirkadian menyebar ke seluruh tubuh dan sebagian organ dan jaringan periferal dapat mengekspresikan osilasi sirkadian secara terisolasi.[28] Dengan demikian, sistem sirkadian seekor binatang menyerupai sebuah toko jam dari pada hanya satu jam saja. Ini telah menimbulkan pertanyaan tentang bagaimana begitu banyak jam dapat disinkronisasi secara efektif.[29]
Biologi sirkadian dan kesehatan manusia
Chronobiology memiliki dampak pada banyak aspek fisiologi kita. Misalnya, jam sirkadian membantu mengatur pola tidur, perilaku makan, pelepasan hormon, tekanan darah dan suhu tubuh (Gambar 3). Jam molekuler juga memainkan peran penting secara lokal di banyak jaringan. Ablasi gen jam pada model hewan menghasilkan produksi hormon yang aritmik, seperti kortikosteron dan insulin.[30] Gen jam juga memberikan pengaruh mendalam pada metabolisme melalui kontrol glukoneogenesis, sensitivitas insulin dan osilasi sistemik glukosa darah.[31] Tidur sangat penting untuk fungsi otak normal dan disfungsi sirkadian telah dikaitkan dengan gangguan tidur, serta depresi, gangguan bipolar, fungsi kognitif, pembentukan memori dan beberapa penyakit neurologis. Dalam kasus yang jarang terjadi, gangguan fase tidur disebabkan oleh mutasi pada gen jam sirkadian yang menghasilkan siklus tidur-bangun yang maju atau tertunda.[32][33] Hasil penelitian telah menunjukkan bahwa gangguan kronis antara gaya hidup kita dan ritme yang didikte oleh jam sirkuler endogen kita mungkin terkait dengan peningkatan risiko berbagai penyakit termasuk kanker, penyakit neurodegeneratif, gangguan metabolisme dan pembengkakan. Upaya sedang dilakukan untuk mengembangkan pendekatan dalam chronobiology dan farmakologi untuk memodifikasi periode, fase atau amplitudo jam sirkadian untuk memperbaiki kesehatan manusia.[34]
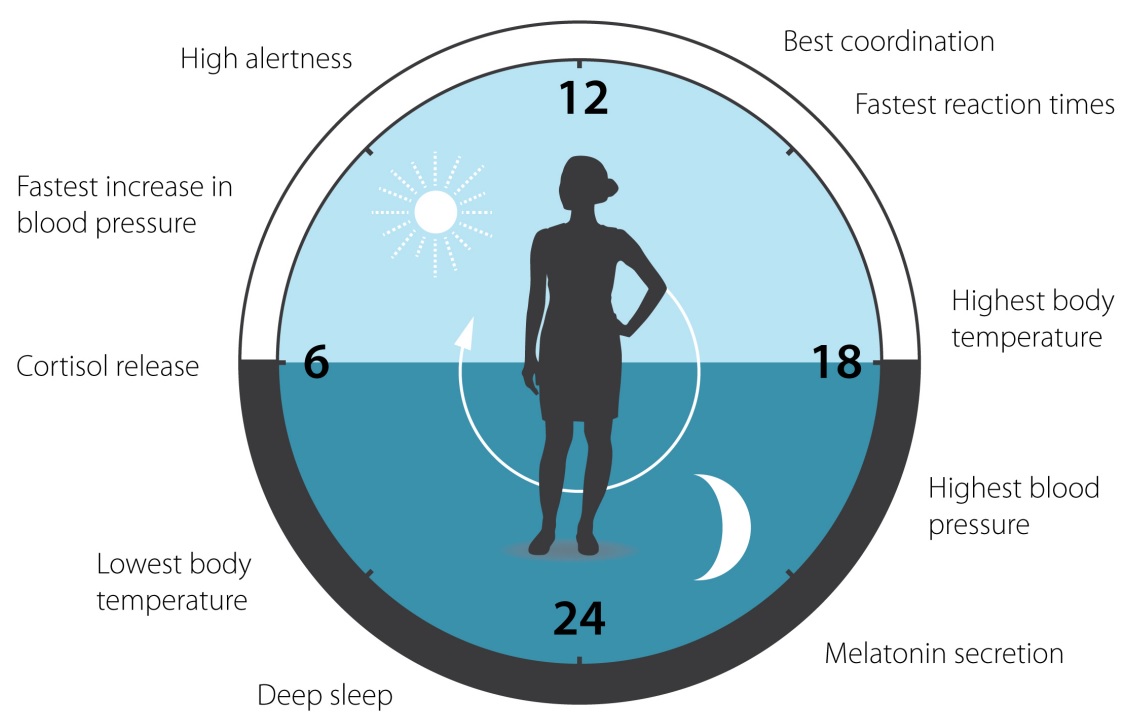
Gambar 3. Jam sirkadian memiliki dampak pada banyak aspek fisiologi kita.
Jam ini membantu mengatur pola tidur, perilaku makan, pelepasan hormon, tekanan darah dan suhu tubuh. Sebagian besar gen kita diatur oleh jam.
Kesimpulan
Penemuan loop umpan balik transkripsi / translasi mandiri sebagai komponen utama mekanisme molekuler di mana gen jam mengendalikan osilasi sirkadian di sel dan jaringan telah menghasilkan paradigma baru dalam pemahaman kita tentang bagaimana organisme mengantisipasi dan menyesuaikan diri dengan isyarat lingkungan sehari-hari contohnya seperti cahaya Sejak penemuan yang dilakukan oleh tiga peraih hadiah Nobel (Hall, Rosbash dan Young), menjelaskan mekanisme fisiologis mendasar, biologi sirkadian telah berkembang menjadi bidang penelitian yang luas dan sangat dinamis, dengan implikasi penting bagi kesehatan dan kesejahteraan kita.
Pengumuman Hadiah Nobel tahun 2017 bidang Fisiologi/Medis ini bisa dilihat di video berikut ini
Sumber : nobelprize.org oleh Profesor Neurosains, Karolinska Institutet Ajun Anggota dari Anggota Komite Nobel dalam Majelis Nobel, Ilustrasi : Mattias Karlén
2. Bidang Fisika
Pada Selasa, 3 Oktober 2017 Komite Nobel untuk Fisika mengumumkan Peraih Hadiah Nobel bidang Fisika tahun 2017 setengah bagian kepada Rainer Weiss, dan setengah lainnya kepada Barry C. Barish serta Kip S. Thorne di Royal Swedish Academy of Sciences sekitar pukul 12.00 waktu Swedia. Ketiganya merupakan fisikawan yang mengerjakan proyek kolaborasi LIGO/VIRGO dalam rangka mendeteksi gelombang gravitasi (konsekuensi dari teori relativitas umum yang pernah diprediksi oleh A. Einstein 100 tahun yang lalu)

Kiri : Rainer Weiss (lahir 29 September 1932), Tengah : Barry C. Barish (lahir 27 Januari 1936), Kanan : Kip S. Thorne (lahir 1 June 1940)
Latar Belakang
Dalam riset yang mereka beri judul "Kicauan Kosmik" pada tanggal 14 September 2015, detektor LIGO di AS melihat ruang bergetar dengan gelombang gravitasi untuk pertama kalinya (lihat Gambar 4). Meski sinyalnya sangat lemah saat mencapai Bumi, hal ini sudah sangat meniru revolusi astrofisika. Gelombang gravitasi adalah cara pandang yang sama sekali baru untuk mengikuti banyak peristiwa di luar angkasa dan menguji batas pengetahuan kita.
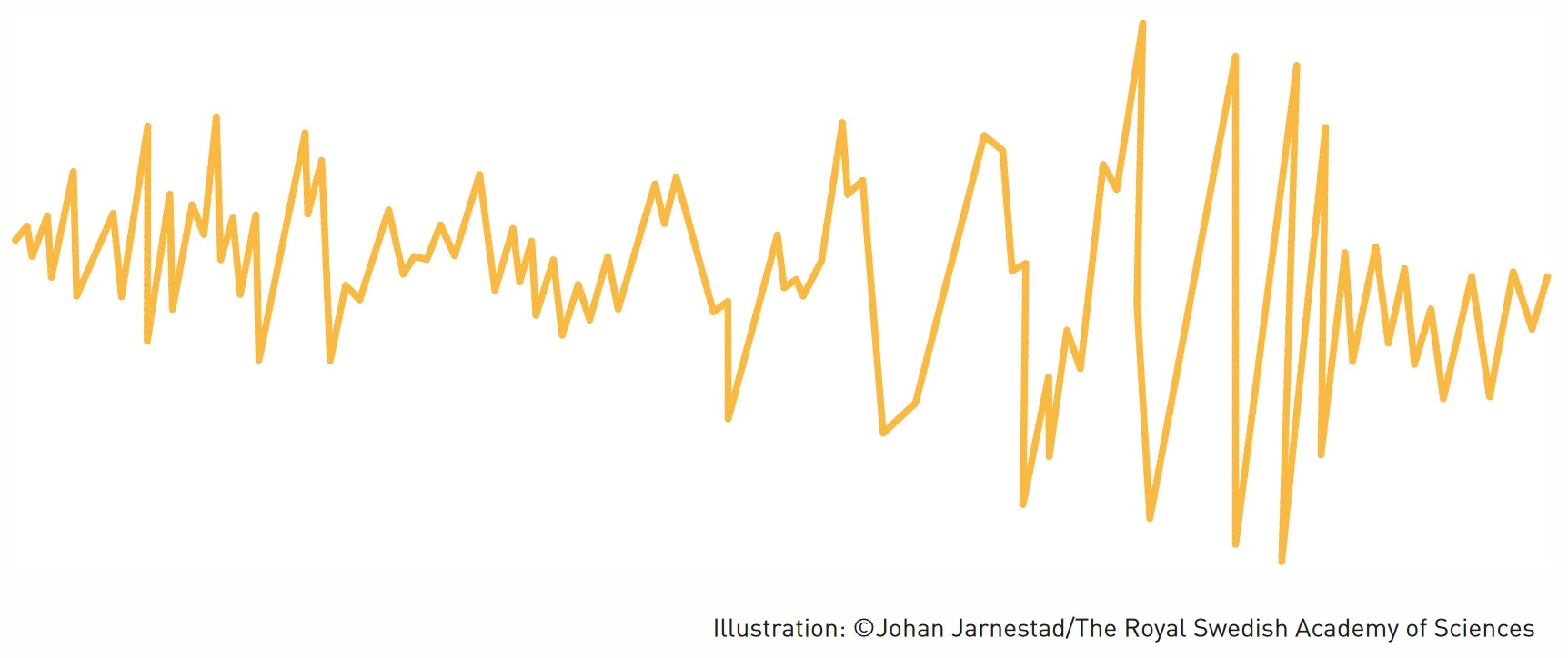
Gambar 4. Plot dari Gelombang gravitasi yang pertama kali pernah dideteksi oleh LIGO.[35]
Gelombang gravitasi yang sekarang telah diamati tercipta dalam tabrakan besar antara dua lubang hitam, lebih dari semilyar tahun yang lalu. SEKALI LAGI !! Albert Einstein benar lagi. Seabad telah berlalu sejak gelombang gravitasi diprediksi oleh teori relativitas umum, tapi dia selalu ragu apakah mereka bisa ditangkap.
LIGO (Laser Interferometer Gravitational-Wave Observatory) adalah proyek kolaborasi dengan lebih seribu peneliti dari lebih dari dua puluh negara. Bersama-sama, mereka telah menyadari sebuah visi yang hampir berusia lima puluh tahun. Pemenang Nobel 2017 memiliki antusiasme dan tekad mereka masing-masing sangat berharga bagi keberhasilan LIGO. Perintis Rainer Weiss dan Kip S. Thorne, bersama dengan Barry C. Barish, ilmuwan dan pemimpin yang membawa proyek ini selesai, telah memastikan bahwa lebih dari empat dekade usaha gelombang gravitasi akhirnya diamati.
Desas-desus mulai beredar sekitar lima bulan sebelum kelompok penelitian internasional selesai menyempurnakan perhitungannya, namun mereka tidak berani mengumumkan temuan mereka sampai 11 Februari 2016. Para peneliti LIGO menetapkan beberapa catatan dengan penemuan pertama mereka. Selain pengamatan gravitasi pertama, keseluruhan peristiwa merupakan indikasi pertama bahwa ruang mengandung lubang hitam berukuran sedang antara 30 dan 60 massa matahari dan dapat digabungkan. Untuk sesaat, radiasi gravitasi dari lubang hitam yang bertabrakan berkali-kali lebih kuat dari pada cahaya yang dikumpulkan dari semua bintang di alam semesta yang terlihat.
Ruang-waktu bergetar
Luar angkasa benar-benar gelap. Tapi tidak sepenuhnya diam. Tremor dari dua lubang hitam bertabrakan mengguncang semua ruang-waktu. Seperti riak dari kerikil yang dilemparkan ke dalam air, gelombang gravitasi dari dampak tabrakannya menyebar melalui kosmos. Butuh waktu bagi mereka untuk mencapai kita di bumi. Meski melaju dengan kecepatan cahaya, (kecepatan tercepat di alam semesta). Mungkin, dibutuhkan lebih dari semilyar tahun agar gelombang ini tiba di Bumi. Pada tanggal 14 September 2015, pukul 11.51 CET, goyangan lembut dalam pola terang di laboratorium kembar LIGO Amerika mengungkapkan drama yang telah berlangsung lama dan jauh, 1,3 miliar tahun cahaya dari Bumi (lihat Gambar 5).
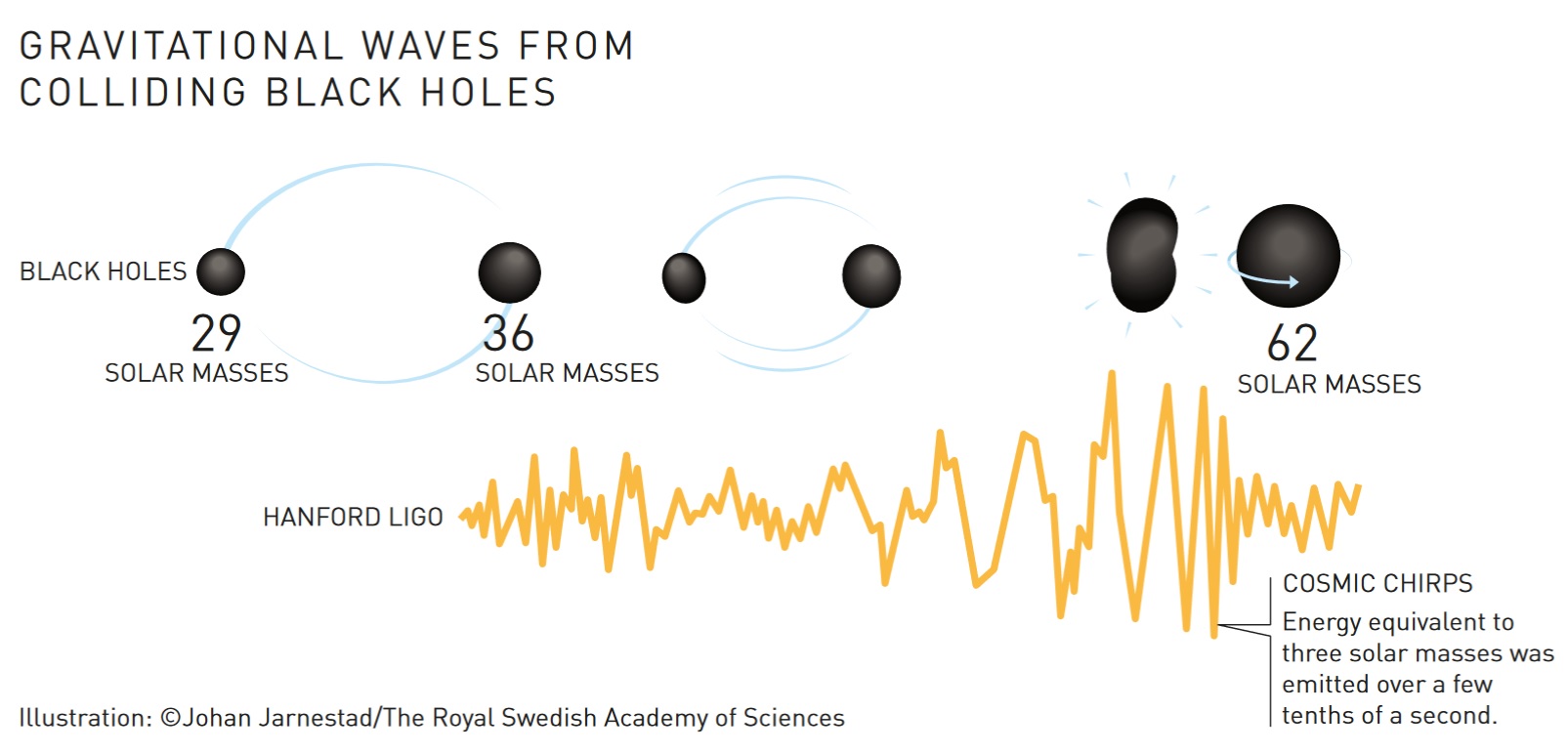
Gambar 5. Kedua lubang hitam memancarkan gelombang gravitasi selama jutaan tahun saat diputar satu sama lain. Mereka semakin dekat, sebelum bergabung menjadi satu lubang hitam dalam beberapa sepersepuluh detik. Gelombang kemudian mencapai crescendo yang, bagi kita di Bumi, 1,3 miliar tahun cahaya cahaya, terdengar seperti kicauan kosmik yang berhenti tiba-tiba.[35]
LIGO bukanlah teleskop biasa untuk mendeteksi cahaya dan radiasi elektromagnetik lainnya dari luar angkasa. Ini adalah instrumen untuk mendengarkan gelombang gravitasi di luar angkasa. Bahkan jika gelombang gravitasi adalah tremor di ruang-waktu sendiri, dan bukan gelombang suara, frekuensinya sama dengan yang dapat kita dengar dengan telinga manusia kita.
Selama beberapa dekade, fisikawan telah mencoba mendeteksi gelombang gravitasi yang mengguncang alam semesta, seperti yang Albert Einstein gambarkan mereka seratus tahun yang lalu. Dia menjelaskan bahwa ruang dan waktu dapat ditempa, dan gabungan empat dimensi ruang-waktu bergetar dengan gelombang gravitasi yang selalu tercipta saat massa melaju (seperti saat pemain ski es menuruni bukit) sebuah bintang meledak di galaksi yang jauh atau sepasang lubang hitam berputar satu sama lain.
Seperti gelombang gravitasi, lubang hitam juga digambarkan oleh teori relativitas umum Einstein dari tahun 1915. Selama lebih dari lima puluh tahun, kebanyakan peneliti tetap yakin bahwa lubang hitam hanya ada sebagai solusi untuk persamaan Einstein, dan sebenarnya tidak berada di luar sana di luar angkasa. Teori relativitas menjelaskan gravitasi sebagai kelengkungan ruang-waktu. Bila gravitasi sangat kuat, kelengkungan bisa menjadi begitu besar sehingga terbentuk lubang hitam. Lubang hitam adalah benda yang paling aneh di ruang-waktu (tidak ada yang bisa melepaskan diri dari mereka) bahkan tidak terang. Oleh karena itu mereka merupakan sumber misterius dalam fisika.
Gelombang gravitasi membawa harapan untuk mengamati sesuatu yang sebelumnya tidak dipikirkan-namun, lama-lama tidak jelas apakah misteri ruang-waktu akan bisa dipecahkan. Selama bertahun-tahun, Albert Einstein yakin tidak akan mungkin mengukur gelombang gravitasi dan tidak yakin apakah ombaknya nyata atau hanya ilusi matematis. Rekan sejawatnya, Arthur Eddington, bahkan lebih skeptis dan menunjukkan bahwa gelombang gravitasi muncul "untuk berkembang dengan kecepatan pemikiran".
Adanya gelombang gravitasi menjadi lebih diterima menjelang akhir tahun 1950an, ketika perhitungan baru menunjukkan bahwa mereka benar-benar membawa energi dan oleh karena itu, pada dasarnya, dapat diukur. Salah satu bukti tidak langsung muncul di tahun 1970an, ketika astronom Amerika Joseph Taylor dan Russell Hulse menggunakan teleskop radio besar untuk mengamati sepasang bintang yang sangat padat, sebuah pulsar ganda. Mereka dapat menunjukkan bahwa bintang-bintang diputar satu sama lain dengan kecepatan tinggi, sementara kehilangan energi dan bergerak lebih dekat bersama-sama. Jumlah energi yang hilang berhubungan dengan perhitungan teoritis untuk gelombang gravitasi. Joseph Taylor dan Russell Hulse dianugerahi Hadiah Nobel dalam Fisika pada tahun 1993.
Namun, mendapatkan bukti langsung tentang gelombang gravitasi memerlukan pengamatan langsung terhadap gelombang. Tapi ruang-waktu yang kaku dan tidak mudah goyah, jadi hanya proses kosmis yang paling kejam yang bisa menyebabkan gelombang gravitasi cukup besar untuk diukur. Namun amplitudonya kecil, mendeteksi mereka seperti mengukur jarak ke bintang sepuluh tahun cahaya dengan presisi setara dengan diameter sehelai rambut. Juga, bahkan jika seluruh alam semesta terus bergetar dengan gelombang gravitasi, kejadian paling eksplosif jarang terjadi di galaksi kita. Kita harus melihat lebih jauh.
Gelombang gravitasi mengungkap masa lalu
Sekarang telah terjadi - gelombang gravitasi telah tertangkap dalam jebakan LIGO. Dua lubang hitam yang akhirnya bertabrakan telah berpindah-pindah satu sama lain sejak penciptaan mereka, di awal sejarah alam semesta. Dengan setiap siklus, mereka menyapu ruang-waktu menjadi spiral, gangguan ruang-waktu yang menyebar lebih jauh dan lebih jauh ke luar angkasa dalam bentuk gelombang gravitasi.
Gelombang ini membawa energi, menyebabkan lubang hitam saling mendekat. Semakin dekat gerakan spiralnya membawa mereka semakin cepat diputar dan semakin banyak energi yang dikirim dalam tarian mempercepat yang berlanjut selama jutaan tahun. Pada akhirnya, dalam sepersekian detik, cakrawala lubang hitam saling bersentuhan, dan lubang-lubang itu berayun menuju ujung yang menentukan pada kecepatan cahaya yang hampir punah. Saat mereka bergabung, semua getarannya hilang, meninggalkan satu lubang hitam berputar tanpa jejak yang terlihat dari awal yang dramatis.
Tapi ingatan tentang persatuan ini tidak sepenuhnya hilang - sejarahnya tetap dalam riak ruang-waktu. Gelombang gravitasi, yang berirama meregangkan dan meremas ruang, mengubah nada saat pesan mereka berubah. Jika kita bisa mendengar semua ombak dan tidak hanya yang terkuat, seluruh alam semesta akan penuh dengan musik, seperti burung berkicau di hutan, dengan nada lebih keras di sini dan yang lebih tenang di sana. Setelah milyaran tahun, saat duo lubang hitam melaju menuju tabrakan terakhir mereka yang kacau, ada sebuah crescendo sebelum nada memudar dalam keheningan yang tidak mengungkapkan apapun.
Hanya beberapa kicauan terakhir yang bisa didengar melalui ruang angkasa. Mengapa mereka begitu pendiam? Ini karena sumber mereka sangat jauh dan gelombang gravitasi, seperti gelombang cahaya, melemah dengan jarak. Jadi ketika gelombang gravitasi tiba di sini, kekuatan mereka telah menurun secara signifikan - peregangan di dalam ruang ruang-waktu yang detektor LIGO harus tangkap saat gelombang yang melintas di Bumi ribuan kali lebih kecil dari inti atom.
LIGO - sebuah interferometer raksasa
Mimpi itu telah ada selama lebih dari lima puluh tahun, dan jalan menuju kesuksesan sudah lama, berkelok-kelok dan terkadang sulit bagi banyak peneliti. Salah satu detektor pertama yang menangkap gelombang gravitasi menyerupai garpu tala, sensitif terhadap gelombang frekuensi tertentu. Tapi Joseph Weber di University of Maryland di Washington hanya bisa menebak frekuensi di mana lubang hitam tersebut akan menyanyikan lagu mereka. Dia membangun detektor pertama di tahun 1960an, namun pada saat itu banyak orang meragukan bahwa gelombang gravitasi dan lubang hitam bahkan ada. Jadi, ini adalah sensasi ketika, di tahun 1970-an, Weber mengaku telah mendengar nada akhir ini. Namun, tidak ada yang bisa mengulangi hasil Weber dan pengamatannya dianggap sebagai alarm palsu.
Pada pertengahan 1970-an, terlepas dari skeptisme yang meluas, Kip Thorne dan Rainer Weiss yakin bahwa gelombang gravitasi dapat dideteksi dan membawa sebuah revolusi dalam pengetahuan kita tentang alam semesta. Rainer Weiss telah menganalisis kemungkinan sumber kebisingan latar belakang yang akan mengganggu pengukuran mereka. Dia juga merancang detektor, interferometer berbasis laser, yang akan mengatasi kebisingan ini.
Sementara Rainer Weiss mengembangkan detektornya di MIT di Cambridge, di luar Boston, Kip Thorne juga mulai bekerja dengan Ronald Drever, yang membangun prototipe pertamanya di Glasgow, Skotlandia. Drever akhirnya pindah untuk bergabung dengan Thorne di Caltech di Los Angeles. Bersama-sama, Weiss, Thorne dan Drever membentuk trio yang memelopori pembangunan selama bertahun-tahun. Drever akhirnya berakhir di luar jalan utama proyek tersebut, namun ia dapat mengalami penemuan pertamanya sebelum meninggal dunia di rumah pada Skotlandia pada bulan Maret 2017.
Alih-alih desain garpu tala Weber, Weiss, Thorne and Drever mengembangkan instrumen lain, berbasis laser interferometer. Prinsipnya sudah lama diketahui, interferometer terdiri dari dua lengan yang membentuk sebuah huruf L. Di sudut dan ujung L, cermin masif ditangguhkan dalam perangkat yang canggih. Gelombang gravitasi yang lewat mempengaruhi lengan interferometer secara berbeda - ketika satu lengan dikompres, yang lain diregangkan.
Sinar laser yang memantul di antara cermin mengukur perubahan pada panjang lengan. Jika tidak ada perubahan yang terjadi, sinar memantul dari laser akan saling membatalkan saat mereka bertemu di sudut L. Namun, jika salah satu lengan interferometer berubah panjang, cahaya bergerak jauh berbeda, sehingga gelombang cahaya kehilangan sinkronisasi dan menghasilkan perubahan intensitas cahaya di mana sinar bertemu (lihat Gambar 6).
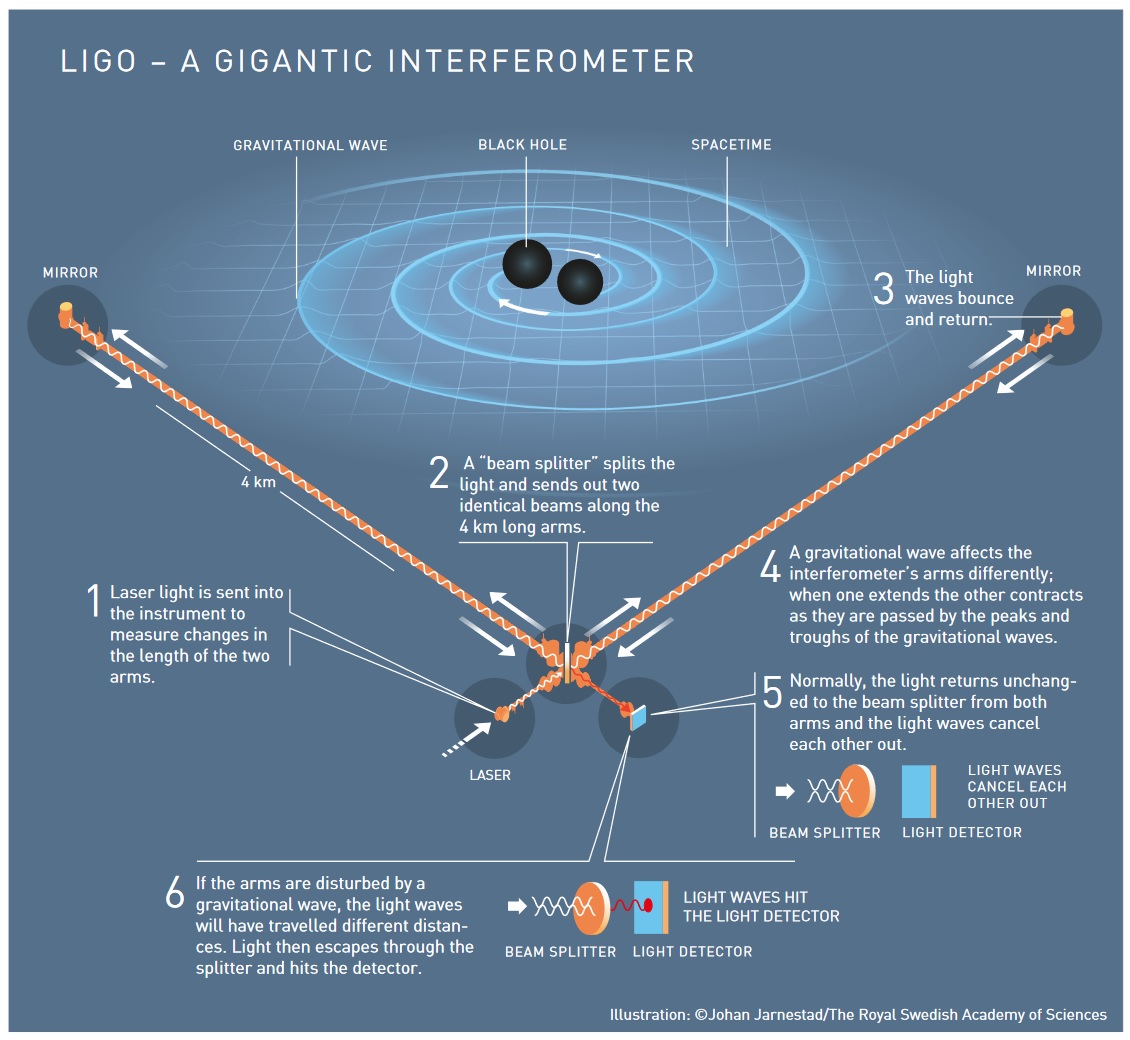
Gambar 6. Bagaimana menangkap gelombang gravitasi. Gelombang gravitasi pertama di dunia diciptakan dalam tabrakan hebat antara dua lubang hitam, 1,3 miliar tahun cahaya jaraknya. Ketika gelombang ini melewati Bumi, 1,3 miliar tahun kemudian, mereka telah melemah secara signifikan: gangguan di ruang-waktu yang diukur LIGO ribuan kali lebih kecil dari inti atom.
Idenya cukup sederhana, tapi lumayan rumit dalam rinciannya, jadi butuh waktu lebih dari empat puluh tahun untuk direalisasikan. Instrumen skala besar diperlukan untuk mengukur perubahan mikroskopis dengan panjang kurang dari inti atom. Rencananya adalah membangun dua interferometer, masing-masing dengan lengan sepanjang empat kilometer dan sinar laser memantul berkali-kali, sehingga memperluas jalan cahaya dan meningkatkan kemungkinan mendeteksi peregangan kecil di ruang-waktu. LIGO terletak di stepa barat laut Amerika Serikat, di luar Hanford, Washington, dengan fasilitas kembar tiga ribu kilometer ke selatan, di rawa-rawa Livingston, Louisiana (lihat Gambar 7).
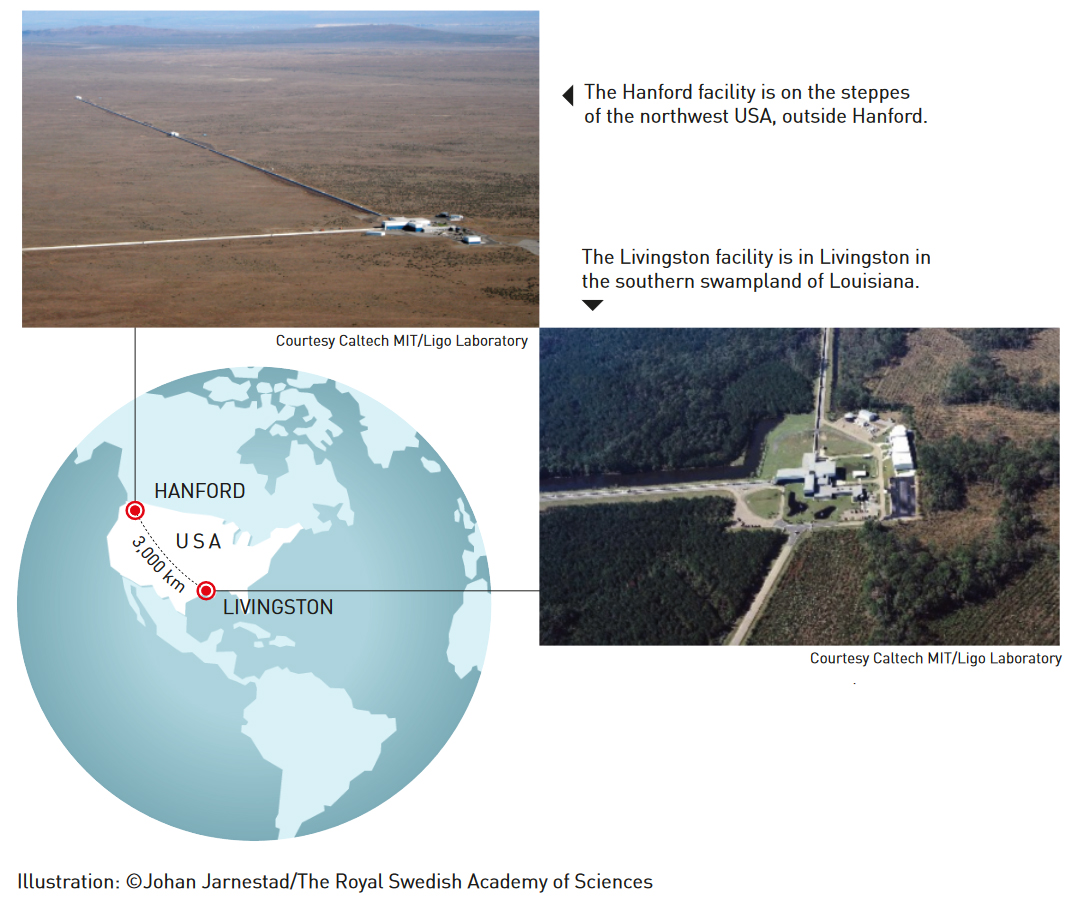
Gambar 7. LIGO terdiri dari dua interferometer identik raksasa. Gelombang gravitasi pertama kali menabrak interferometer di Livingston dan kemudian melewati kembarannya di Hanford, lebih dari 3.000 km jauhnya, 7 milidetik kemudian. Sinyal hampir sama, dan cocok dengan sinyal yang diprediksi untuk gelombang gravitasi. Dengan menggunakan sinyal, area di langit selatan juga bisa diidentifikasi sebagai daerah gelombang.
Butuh waktu bertahun-tahun mengembangkan alat yang paling sensitif untuk bisa membedakan gelombang gravitasi dari semua kebisingan di latar belakang. Ini memerlukan analisis dan teori lanjutan yang canggih, yang menurut Kip Thorne hanya bisa dilakukan oleh ilmuwan yang sangat ahli. Tetapi tingkat teknik dan pengerjaan kreatif tertinggi diperlukan untuk membangun instrumen yang cerdik, dan inilah kontribusi perintis Rainer Weiss. Panjang dan intensitas cahaya laser harus setepat mungkin, dan sinar harus menabrak cermin yang ditangguhkan dengan tepat. Mereka seharusnya tidak gemetar sama sekali, bahkan saat daun jatuh dari pohon terdekat, anak kecil melewatinya atau sebuah truk melewati jalan yang jauh. Pada saat yang sama, cermin gantung ini harus bebas diayunkan dengan gelombang gravitasi. Gerakan termal atom pada permukaan cermin harus dikompensasi, serta efek kuantum pada laser. Perlu untuk mengembangkan teknologi laser baru dan menciptakan material baru, serta membangun tabung vakum raksasa, isolasi seismik dan teknologi vital lainnya yang jauh melampaui apa yang telah dicapai sebelumnya.
Menjalankan proyek semacam itu dalam skala kecil tidak mungkin lagi dilakukan dan pendekatan baru diperlukan. Pada tahun 1994, ketika Barry Barish mengambil alih jabatan sebagai pemimpin LIGO, dia mengubah kelompok riset kecil sekitar 40 orang menjadi sebuah kolaborasi internasional berskala besar dengan lebih dari seribu peserta. Dia mencari keahlian yang diperlukan dan membawa banyak kelompok penelitian dari berbagai negara. Impian yang tidak mungkin yang hanya bisa terwujud melalui upaya kolaborasi sains besar.
Sinyal tiba segera
Pada bulan September 2015, LIGO hendak memulai lagi setelah upgrade yang telah berlangsung beberapa tahun. Kini dilengkapi dengan laser sepuluh kali lipat lebih kuat, cermin seberat 40 kg, penyaringan noise yang sangat canggih, dan salah satu sistem vakum terbesar di dunia, ia menangkap sinyal gelombang beberapa hari sebelum percobaan dimulai secara resmi. Gelombang pertama melewati fasilitas Livingston dan 7 milidetik kemudian - bergerak dengan kecepatan cahaya - ia muncul di Hanford, tiga ribu kilometer jauhnya.
Sebuah pesan dari sistem komputerisasi dikirim pagi-pagi pada tanggal 14 September 2015. Semua orang di AS sedang tidur, namun di Hannover di Jerman pukul 11.51 dan Marco Drago, seorang fisikawan muda di Institut Max Planck untuk Fisika Gravitasi, sedang bersiap-siap untuk makan siang. Lekuk yang dilihatnya persis seperti yang telah dia praktikkan, begitu sering dikenali. Mungkinkah dia benar-benar orang pertama di dunia yang melihat gelombang gravitasi? Atau apakah itu hanya alarm palsu, salah satu tes buta sesekali yang hanya sedikit orang yang tahu?
Bentuk gelombang persis seperti yang diprediksi, dan itu bukan tes. Semuanya pas dengan sempurna. Perintisnya, sekarang berusia 80-an, dan rekan LIGO mereka akhirnya bisa mendengar musik impian mereka, seperti glissando, atau seekor burung yang berkicau dengan lagu soliternya. Itu hampir terlalu bagus untuk menjadi kenyataan, tapi baru pada bulan Februari tahun berikutnya mereka diizinkan untuk mengungkapkan berita itu kepada siapapun, bahkan keluarga mereka.
Rahasia yang disebut GW 150914 memenuhi semua harapan mereka.[36] Dari sinyal tersebut, peneliti bisa mengetahui bahwa lubang hitam itu 29 dan 36 kali lebih berat dari pada Matahari, tapi diameternya dibanding diameter matahari hanya lebih besar tidak kurang dari 200 kilometer. Mereka bergabung untuk membentuk lubang hitam sekitar 62 kali massa matahari, sehingga selama beberapa sepersepuluh detik mereka mampu memancarkan energi dalam bentuk gelombang gravitasi yang setara dengan tiga kali massa matahari. Hal ini membuat GW 150914 menjadi objek bercahaya paling kuat di alam semesta untuk saat yang singkat itu. Sinyal tersebut juga mengindikasikan daerah di langit selatan di mana peristiwa kekerasan terjadi, 1,3 miliar tahun cahaya jauhnya. Ini berarti tabrakan itu terjadi 1,3 miliar tahun yang lalu, pada saat kehidupan di Bumi mengambil langkah dari organisme uniseluler ke multiselular.
LIGO telah mengamati dua peristiwa serupa lainnya sejak penemuan pertama. Fasilitas lainnya di Eropa, VIRGO, di luar Pisa, Italia, bergabung dengan LIGO pada bulan Agustus 2017 dan mereka mengumumkan penemuan kolaboratif pertama mereka pada tanggal 27 September. Ketiga detektor tersebut mengamati gelombang gravitasi kosmik yang sama pada 14 Agustus 2017. Mereka berasal dari dua lubang hitam berukuran menengah yang bertabrakan 1,8 miliar tahun yang lalu.
Detektor sekarang telah melihat alam semesta bergetar empat kali dan masih banyak lagi penemuan yang diharapkan. India[37] dan Jepang juga membangun observatorium gelombang gravitasi baru. Dengan beberapa eksperimen yang berjarak jauh, peneliti harus bisa mengidentifikasi dari mana asal sinyal tersebut. Pengamatan gelombang gravitasi kemudian dapat diikuti oleh studi yang menggunakan teleskop optik, teleskop sinar-X, atau jenis teleskop lainnya.
Sejauh ini semua jenis radiasi elektromagnetik dan partikel, seperti sinar kosmik atau neutrino, telah memberi kita pengetahuan tentang alam semesta. Gelombang gravitasi, bagaimanapun, adalah kesaksian langsung terhadap gangguan di ruang-waktu itu sendiri. Ini adalah sesuatu yang benar-benar baru dan berbeda, membuka dunia yang tak terlihat. Banyak penemuan menanti mereka yang berhasil menangkap gelombang gravitasi dan menafsirkan pesan mereka. Tim100 sendiri pernah membahas pendeteksian ini tahun lalu (selengkapnya baca di sini : Deteksi Gelombang Gravitasi setelah 100 tahun prediksi)
Pengumuman Hadiah Nobel tahun 2017 bidang Fisika ini bisa dilihat di video berikut ini
Sumber : nobelprize.org oleh : Joanna Rose, Editor : Olga Botner dan Gunnar Ingelman (Komite Nobel bidang Fisika), ilustrasi : Johan Jarnestad (Royal Swedish Academy of Sciences)
3. Bidang Kimia
Sementara pada hari Rabu, 4 Oktober 2017 Hadiah Nobel di bidang Kimia diberikan kepada Jacques Dubochet, Joachim Frank dan Richard Henderson atas pengembangan mikroskop krio-elektron untuk penentuan resolusi tinggi struktur biomolekul dalam larutan. Dengan menggunakan mikroskop krio-elektron, para periset sekarang dapat membekukan biomolekul pada pertengahan gerakan dan menggambarkannya pada resolusi atom. Teknologi ini telah membawa biokimia ke era baru.

Kanan : Jacques Dubochet (lahir Oktober 1941), Tengah : Joachim Frank (lahir 12 September 1940) dan Kiri : Richard Henderson (lahir 19 Juli 1945)
Selama beberapa tahun terakhir, banyak struktur molekul kehidupan yang menakjubkan telah memenuhi literatur ilmiah (gambar 8): Jarum injeksi Salmonella untuk menyerang sel; protein yang memberikan ketahanan terhadap kemoterapi dan antibiotik; molekul kompleks yang mengatur irama sirkadian, reaksi kompleks penangkap cahaya untuk fotosintesis dan sensor tipe tekanan yang memungkinkan kita mendengarnya. Ini hanya beberapa contoh dari ratusan biomolekul yang sekarang telah dicitrakan dengan menggunakan mikroskop krio-elektron (cryo-EM).
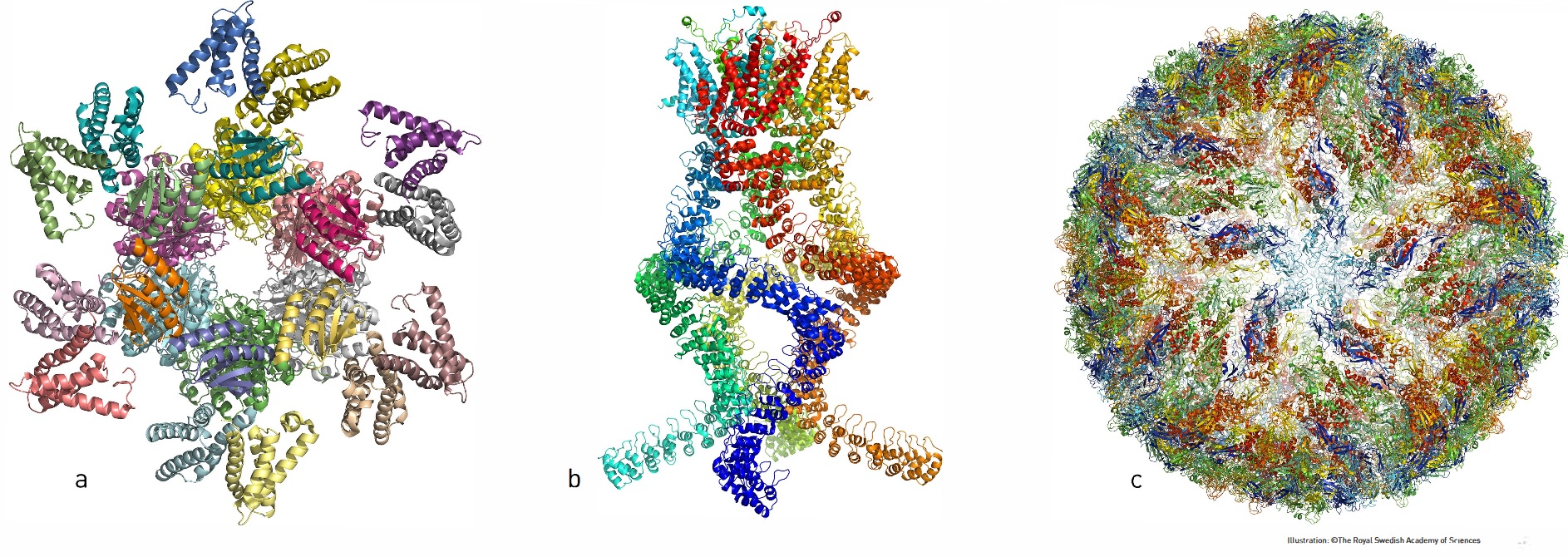
Gambar 8. Selama beberapa tahun terakhir, periset telah menerbitkan struktur atom dari banyak protein kompleks. a. Protein kompleks yang mengatur ritme sirkadian. b. Sensor tipe yang membaca perubahan tekanan di telinga dan memungkinkan kita untuk mendengar. c. Virus Zika.
Ketika para periset mulai menduga bahwa virus Zika menyebabkan epidemi bayi baru lahir yang rusak otaknya di Brasil, mereka beralih ke cryo-EM untuk memvisualisasikan virus tersebut. Selama beberapa bulan, gambar tiga dimensi (3D) virus pada resolusi atom dihasilkan dan para periset dapat mulai mencari target potensial untuk obat-obatan. Jacques Dubochet, Joachim Frank dan Richard Henderson telah membuat terobosan penemuan yang memungkinkan pengembangan cryo-EM. Metode ini telah membawa biokimia ke era baru, sehingga lebih mudah dari pada sebelumnya untuk menangkap gambar biomolekul.
Gambar - kunci penting untuk pengetahuan
Pada paruh pertama abad ke-20, biomolekul - protein, DNA dan RNA - menjadi terra incognita pada peta biokimia. Para ilmuwan tahu mereka memainkan peran mendasar di dalam sel, namun tidak tahu seperti apa penampilan mereka. Baru pada tahun 1950an, ketika para periset di Cambridge mulai mengekspos kristal protein ke sinar X, hal tersebut merupakan yang pertama yang memungkinkan untuk memvisualisasikan struktur bergelombang dan spiral dari protein.
Pada awal 1980an, penggunaan kristalografi sinar-X dilengkapi dengan penggunaan spektroskopi resonansi magnetik nuklir (nuclear magnetic resonance NMR) untuk mempelajari protein dalam keadaan padat dan dalam larutan. Teknik ini tidak hanya mengungkap struktur mereka, tapi juga bagaimana mereka bergerak dan berinteraksi dengan molekul lain.
Berkat kedua metode ini, sekarang ada database yang berisi ribuan model biomolekul yang digunakan dalam segala hal mulai dari riset dasar hingga pengembangan farmasi. Namun, kedua metode tersebut memiliki keterbatasan mendasar. NMR dalam larutan hanya bekerja untuk protein yang relatif kecil. Kristalografi sinar-X mengharuskan molekul membentuk kristal yang terorganisir dengan baik, seperti saat air membeku menjadi es. Gambarnya seperti potret hitam dan putih dari kamera awal - pose kaku mereka sedikit menunjukkan sedikit tentang dinamika protein. Juga, banyak molekul gagal mengatur diri mereka sendiri dalam kristal, yang menyebabkan Richard Henderson meninggalkan kristalografi sinar-X pada tahun 1970an - dan ini adalah di mana kisah Hadiah Nobel tahun 2017 di bidang Kimia dimulai.
Masalah dengan kristal membuat Henderson berganti jalur
Richard Henderson menerima gelar doktornya dari bidang kristalografi sinar-X, Cambridge, Inggris. Dia menggunakan metode pencitraan untuk protein, namun kemunduran muncul saat dia mencoba mengkristal protein yang secara alami tertanam di membran yang mengelilingi sel.
Protein membran sulit dikelola. Ketika mereka dikeluarkan dari lingkungan alami mereka - membran - mereka sering mengelompok menjadi massa yang tidak berguna. Protein membran pertama yang dikerjakan Richard Henderson dengan susah menghasilkan dalam jumlah yang cukup; yang kedua gagal mengkristal. Setelah bertahun-tahun kecewa, dia beralih ke satu-satunya alternatif yang tersedia: mikroskop elektron.
Hal ini terbuka untuk diskusi apakah mikroskop elektron benar-benar pilihan saat ini. Transmisi mikroskop elektron, bekerja lebih atau kurang seperti mikroskop biasa, namun seberkas elektron dikirim melalui sampel dan bukan cahaya. Panjang gelombang elektron jauh lebih pendek dari pada cahaya, sehingga mikroskop elektron dapat membuat struktur sangat kecil terlihat - bahkan posisi atom individu.
Secara teori, resolusi mikroskop elektron lebih dari cukup bagi Henderson untuk mendapatkan struktur atom protein membran, namun dalam praktiknya proyek ini hampir tidak mungkin. Ketika mikroskop elektron ditemukan pada tahun 1930an, para ilmuwan berpikir bahwa itu hanya cocok untuk mempelajari materi mati. Sinar elektron yang kuat yang diperlukan untuk mendapatkan gambar beresolusi tinggi membakar bahan biologis dan, jika berkas dilemahkan, citra kehilangan kontrasnya dan menjadi tidak jelas.
Selain itu, mikroskop elektron membutuhkan vakum, suatu kondisi di mana biomolekul memburuk karena air di sekitarnya menguap. Ketika biomolekul mengering, mereka runtuh dan kehilangan struktur alami mereka, membuat gambar menjadi tidak berguna. Hampir semuanya menunjukkan bahwa Richard Henderson akan gagal, namun proyek tersebut berhasil diselamatkan oleh protein khusus yang telah dia pilih untuk dipelajari: bacteriorhodopsin.
Yang terbaik sejauh ini tidak cukup baik untuk Henderson
Bacteriorhodopsin adalah protein berwarna ungu yang tertanam dalam membran organisme fotosintesis, di mana ia menangkap energi dari sinar matahari. Alih-alih mengeluarkan protein sensitif dari membran, seperti yang sebelumnya Richard Henderson coba lakukan, dia dan rekannya mengambil membran ungu yang lengkap dan meletakkannya di bawah mikroskop elektron. Ketika protein tetap dikelilingi oleh membran, ia mempertahankan strukturnya; Mereka menutupi permukaan sampel dengan larutan glukosa yang melindunginya dari pengeringan dalam ruang hampa.
Sinar elektron yang keras merupakan masalah utama, namun para periset menggunakan bagaimana molekul bakteri dalam molekulnya dikemas dalam membran organisme. Alih-alih peledakan itu dengan dosis penuh elektron, mereka memiliki aliran balok yang lebih lemah melalui sampel. Kontras gambar itu buruk dan mereka tidak dapat melihat molekul individu, namun mereka menggunakan fakta bahwa protein secara teratur dikemas dan berorientasi ke arah yang sama. Ketika semua protein membaurkan berkas elektron dengan cara yang hampir sama, mereka dapat menghitung gambar yang lebih rinci berdasarkan pola difraksi - mereka menggunakan pendekatan matematis serupa dengan yang digunakan dalam kristalografi sinar-X.
Pada tahap berikutnya, para peneliti membalikkan membran di bawah mikroskop elektron, memotret dari berbagai sudut. Dengan cara ini, pada tahun 1975 adalah mungkin untuk menghasilkan model 3D kasar dari struktur bacteriorhodopsin (gambar 9), yang menunjukkan bagaimana rantai protein bergoyang-goyang melalui membran tujuh kali.
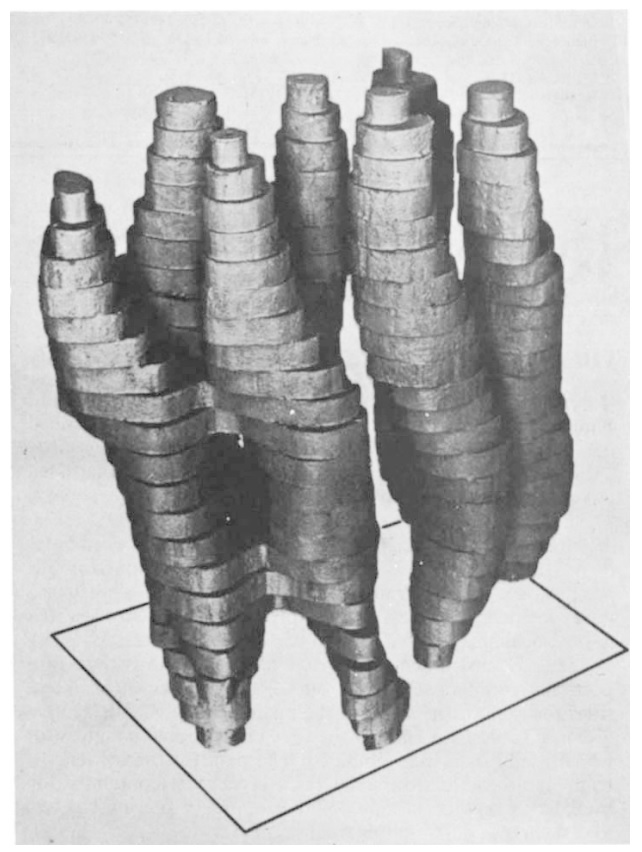
Gambar 9. Model kasar pertama bacteriorhodopsin, diterbitkan pada tahun 1975. Gambar diambil dari Nature 257: 28-32.
Itu adalah gambaran terbaik dari protein yang pernah dihasilkan dengan menggunakan mikroskop elektron. Banyak orang terkesan dengan resolusi tersebut, yaitu 7 Ångström (0.000 0007 milimeter), tapi ini tidak cukup bagi Richard Henderson. Tujuannya adalah untuk mencapai resolusi yang sama seperti yang diberikan oleh kristalografi sinar-X, yaitu sekitar 3 Ångström, dan dia yakin bahwa mikroskop elektron bisa lebih banyak memberi.
Henderson menghasilkan gambar pertama dengan resolusi atom
Selama tahun-tahun berikutnya, mikroskop elektron berangsur-angsur membaik. Lensa menjadi lebih baik dan cryotechnology dikembangkan (kami akan kembali ke ini), di mana sampel didinginkan dengan nitrogen cair selama pengukuran, melindungi mereka dari kerusakan oleh berkas elektron.
Richard Henderson secara bertahap menambahkan rincian lebih lanjut tentang model bacteriorhodopsin. Untuk mendapatkan gambar paling tajam ia melakukan perjalanan ke mikroskop elektron terbaik di dunia. Mereka semua memiliki kelemahan, tapi saling melengkapi. Akhirnya, di 1990, 15 tahun setelah dia mempublikasikan model pertama, Henderson mencapai tujuannya dan mampu menyajikan struktur bacteriorhodopsin pada resolusi atom (gambar 10).[38]
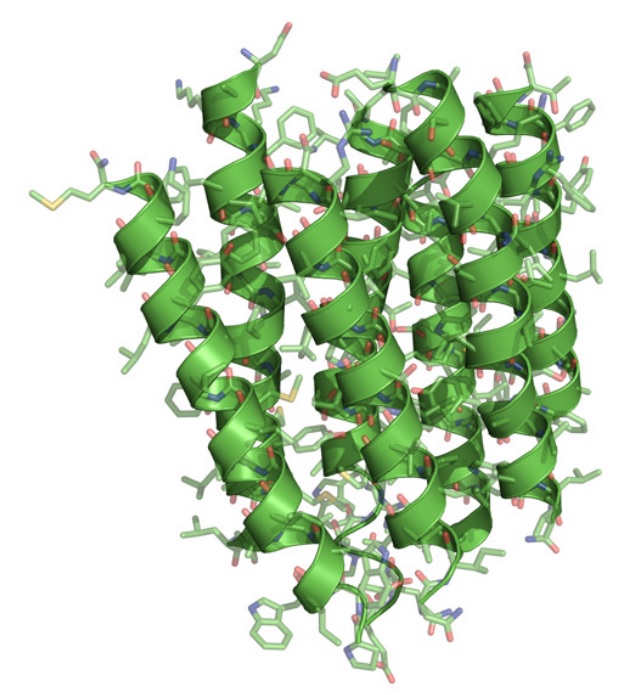
Gambar 10. Pada tahun 1990, Henderson mempresentasikan struktur bacteriorhodopsin pada resolusi atom.
Dengan demikian ia membuktikan bahwa cryo-EM dapat menyediakan gambar sedetil mungkin yang dihasilkan dengan menggunakan kristalografi sinar-X, yang merupakan tonggak penting. Namun, kemajuan ini dibangun di atas pengecualian: bagaimana protein secara alami dikemas sendiri secara teratur di membran. Beberapa protein lain secara spontan memerintahkan diri mereka dengan cara ini. Pertanyaannya adalah apakah metode itu dapat digeneralisasi: mungkinkah menggunakan mikroskop elektron untuk menghasilkan gambar 3D resolusi tinggi protein yang secara acak berserakan dalam sampel dan berorientasi pada arah yang berbeda? Richard Henderson yakin itu akan terjadi, sementara yang lain menganggap ini adalah utopia.
Di Departemen Kesehatan Negara Bagian New York, Joachim Frank telah lama bekerja untuk menemukan solusi untuk masalah itu. Pada tahun 1975, ia mempresentasikan sebuah strategi teoretis di mana informasi yang tampaknya minim ditemukan dalam gambar dua dimensi mikroskop elektron bisa digabung untuk menghasilkan resolusi tinggi, tiga dimensi utuh. Butuh waktu lebih dari satu dekade untuk mewujudkan gagasan ini.
Frank memperbaiki analisis citra
Strategi Joachim Frank (lihat gambar 11) dibangun di atas komputer yang membedakan antara protein yang diposisikan secara acak dan latar belakang gambar mikroskop elektron dari proteinnya dibuat kabur. Dia mengembangkan metode matematis yang memungkinkan komputer mengenali pola berulang yang berbeda pada gambar. Komputer kemudian menyortir pola serupa ke dalam kelompok yang sama dan menggabungkan informasi dalam gambar ini untuk menghasilkan citra rata-rata yang lebih tajam. Dengan cara ini ia memperoleh sejumlah resolusi tinggi, dua dimensi gambar yang menunjukkan protein yang sama namun dari berbagai sudut. Algoritma untuk perangkat lunak selesai pada tahun 1981.
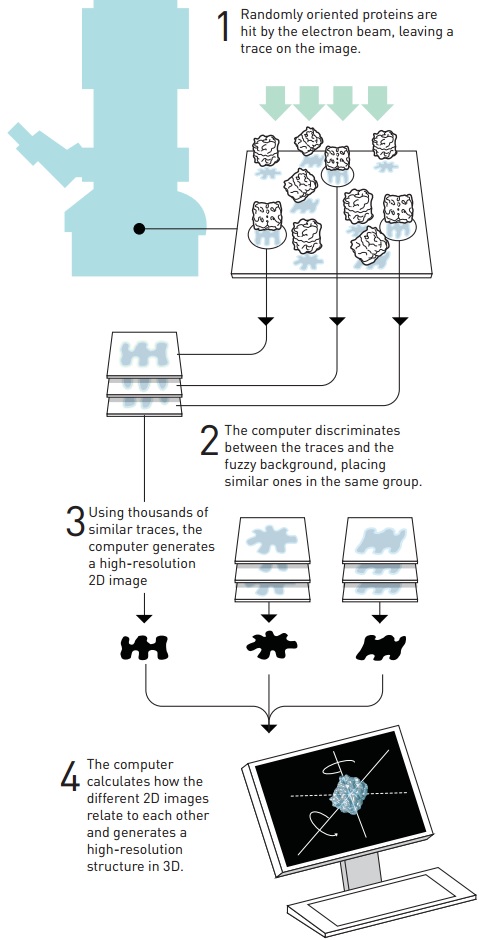
Gambar 11. Analasis gambar oleh Frank untuk struktur 3 dimensi.
Langkah selanjutnya adalah menentukan secara matematis bagaimana gambar dua dimensi yang berbeda saling terkait satu sama lain, dan berdasarkan hal ini, untuk membuat gambar 3D. Frank menerbitkan bagian dari metode analisis citra ini pada pertengahan 1980an dan menggunakannya untuk menghasilkan model permukaan ribosom, mesin molekuler raksasa yang membangun protein di dalam sel.
Metode pengolahan gambar Joachim Frank sangat penting untuk pengembangan cryo-EM. Sekarang kita akan melompat beberapa tahun ke depan - pada tahun 1978, bersamaan dengan saat Frank menyempurnakan program komputernya, Jacques Dubochet direkrut ke Laboratorium Biologi Molekuler Eropa di Heidelberg untuk memecahkan masalah dasar mikroskop elektron lainnya: bagaimana Sampel biologis mengering dan rusak saat terkena vakum.
Dubochet membuat gelas dari air
Pada tahun 1975, Henderson menggunakan larutan glukosa untuk melindungi membrannya dari dehidrasi, namun metode ini tidak bekerja untuk biomolekul yang larut dalam air. Peneliti lain telah mencoba membekukan sampel karena es menguap lebih lambat dari pada air, namun kristal es mengganggu berkas elektron sehingga banyak gambar itu tidak ada gunanya.
Air yang menguap merupakan dilema utama. Namun, Jacques Dubochet melihat solusi potensial: mendinginkan air dengan sangat cepat sehingga memantapkannya. Bentuk cairnya membentuk kaca bukan kristal. Kaca tampaknya merupakan bahan padat, tapi sebenarnya cairan karena memiliki molekul yang tidak teratur. Dubochet menyadari bahwa jika dia bisa mendapatkan air untuk membentuk gelas - juga dikenal sebagai air vitrifikasi - berkas elektron akan terdispersikan secara merata dan memberikan latar belakang seragam.
Awalnya, kelompok penelitian berusaha melakukan vitrifikasi tetesan air kecil dalam nitrogen cair pada suhu -196 ° C, namun berhasil hanya bila mereka mengganti nitrogen dengan etana yang pada gilirannya telah didinginkan oleh nitrogen cair. Di bawah mikroskop mereka melihat setetes yang tidak seperti yang pernah mereka lihat sebelumnya. Mereka pertama kali berasumsi bahwa itu etana, tapi ketika tetesan itu sedikit menghangat, molekul-molekul itu tiba-tiba mengatur kembali tubuhnya dan membentuk struktur kristal es yang sudah dikenal. Itu adalah sebuah kemenangan - terutama karena beberapa periset telah mengklaim bahwa tidak mungkin untuk mengurangi tetesan air. Kita sekarang percaya bahwa air vitrifikasi adalah bentuk air yang paling umum di alam semesta.[39]
Sebuah teknik sederhana untuk kontras
Setelah terobosan pada tahun 1982, kelompok penelitian Dubochet dengan cepat mengembangkan teknik yang masih digunakan dalam cryo-EM (gambar 12). Mereka membubarkan sampel biologis mereka - pada awalnya berbeda bentuk virus - dalam air. Solusinya kemudian disebarkan di atas jaring logam halus sebagai film tipis. Dengan menggunakan konstruksi mirip busur, mereka menembakkan jaring ke etana cair sehingga lapisan tipis air menjadi tervitrifikasi.
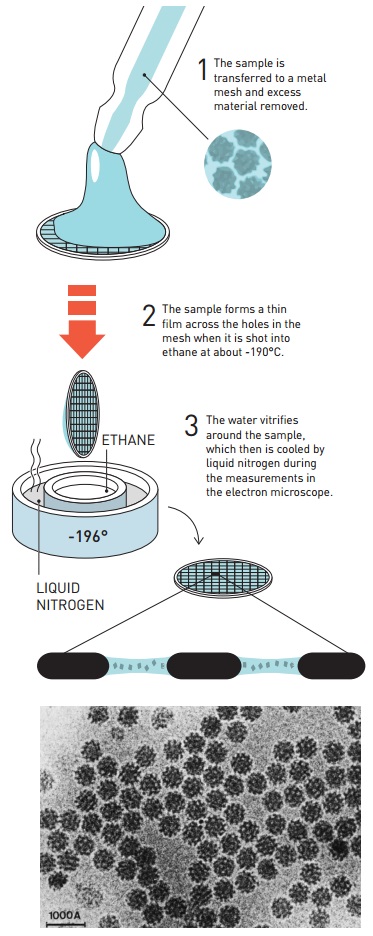
Gambar 12. Metode verifikasi Dubochet
Pada tahun 1984, Jacques Dubochet menerbitkan gambar pertama dari sejumlah virus yang berbeda, bulat dan heksagonal, yang ditunjukkan dalam kontras yang tajam dengan latar belakang air vitrifikasi. Bahan biologis sekarang dapat dengan mudah disiapkan untuk mikroskop elektron, dan peneliti segera mengetuk pintu Dubochet untuk mempelajari teknik baru ini.
Dari blobologi sampai revolusi
Bagian terpenting dari cryo-EM ada pada tempatnya, namun gambarnya masih memiliki resolusi yang buruk. Pada tahun 1991, ketika Joachim Frank menyiapkan ribosom menggunakan metode vitrifikasi Dubochet dan menganalisis gambar dengan perangkat lunaknya sendiri, ia memperoleh struktur 3D yang memiliki resolusi 40 Å. Dulu sebuah langkah maju yang luar biasa untuk mikroskop elektron, namun gambar itu hanya menunjukkan kontur ribosom. Terus terang, itu tampak seperti gumpalan dan gambar bahkan tidak mendekati resolusi atom kristalografi sinar-X.
Karena cryo-EM jarang bisa memvisualisasikan sesuatu selain permukaan yang tidak rata, metode ini terkadang disebut "blobologi". Namun, setiap perangkat dalam mikroskop elektron secara bertahap telah dioptimalkan, karena Richard Henderson dengan sangat gigih mempertahankan visinya bahwa mikroskop elektron suatu hari akan secara rutin memberikan gambar yang menunjukkan atom individu. Resolusi telah ditingkatkan, Ångström demi Ångström, dan rintangan teknis terakhir diatasi pada tahun 2013, ketika jenis detektor elektron baru mulai digunakan (gambar 13).[40]
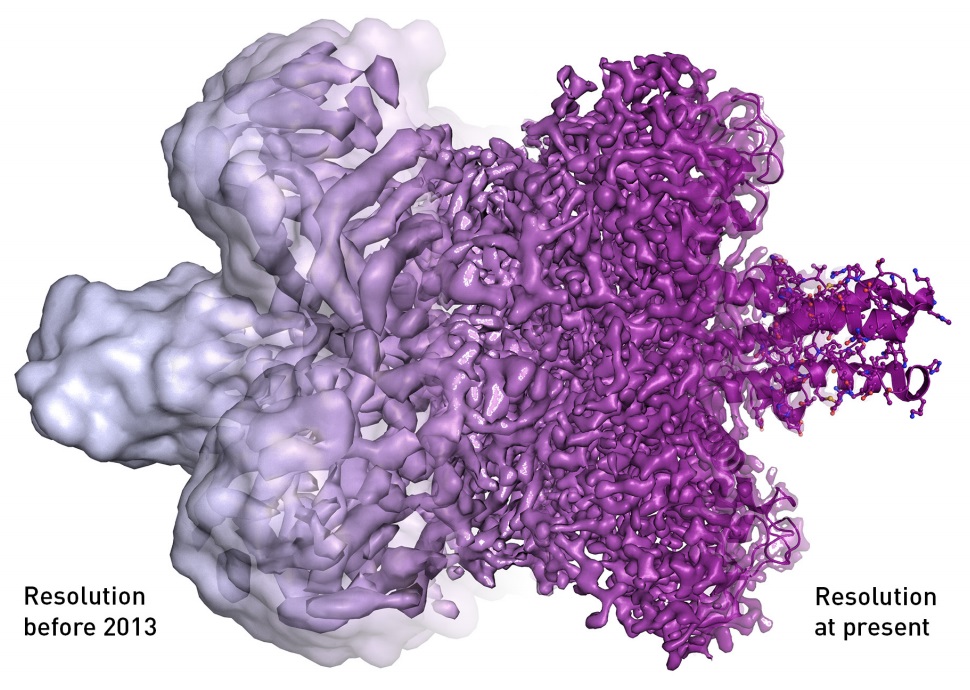
Gambar 13. Resolusi mikroskop elektron telah meningkat secara radikal dalam beberapa tahun terakhir, dari kebanyakan menunjukkan gumpalan tak berbentuk hingga sekarang mampu memvisualisasikan protein pada resolusi atom. Gambar: Martin Högbom.
Setiap sudut tersembunyi sel bisa dieksplorasi
Sekarang mimpinya menjadi kenyataan, dan kita menghadapi perkembangan eksplosif dalam biokimia. Ada sejumlah manfaat yang membuat cryo-EM begitu revolusioner: Metode vitrifikasi Dubochet relatif mudah digunakan dan membutuhkan ukuran sampel minimal. Karena proses pendinginan yang cepat, biomolekul dapat dibekukan pada pertengahan aksi dan para periset dapat mengambil rangkaian gambar yang menangkap berbagai bagian proses. Dengan cara ini, mereka menghasilkan 'film' yang mengungkapkan bagaimana protein bergerak dan berinteraksi dengan molekul lain.
Menggunakan cryo-EM, juga lebih mudah dari pada sebelumnya untuk menggambarkan protein membran, yang sering berfungsi sebagai target obat-obatan, dan molekul kompleks besar. Namun, protein kecil tidak dapat dipelajari dengan mikroskop elektron, namun dapat divisualisasikan dengan spektroskopi NMR atau kristalografi sinar-X.
Setelah Joachim Frank mempresentasikan strategi untuk metode pengolahan citra secara umum pada tahun 1975, seorang peneliti menulis: "Jika metode seperti itu disempurnakan, maka, menurut kata-kata salah satu ilmuwan, langit akan menjadi batasnya."
Sekarang kita di sana - langit adalah batasnya. Jacques Dubochet, Joachim Frank dan Richard Henderson, melalui penelitian mereka, membawa "manfaat terbesar bagi umat manusia." Setiap sudut sel dapat ditangkap secara detail dan biokimia ditetapkan untuk masa depan yang menggairahkan.
Pengumuman Hadiah Nobel tahun 2017 bidang Kimia ini bisa dilihat di video berikut ini
Sumber : nobelprize.org oleh : Ann Fernholm, editor : Peter Brzezinski, Gunnar von Heijne dan Sara Snogerup Linse (Komite Nobel di bidang Kimia), ilustrasi : Johan Jarnestad (Royal Swedish Academy of Sciences)
Daftar Pustaka
[1] Konopka, R.J., and Benzer, S. 1971. Clock mutants of Drosophila melanogaster. Proc Natl Acad Sci USA 68, 2112–2116.
[2] Bargiello, T.A., and Young, M.W. 1984. Molecular genetics of a biological clock in Drosophila. Proc Natl Acad Sci USA 81, 2142–2146
[3] Bargiello, T.A., Jackson, F.R., and Young, M.W. 1984. Restoration of circadian behavioural rhythms by gene transfer in Drosophila. Nature 312, 752–754
[4] Reddy, P., Zehring, W.A., Wheeler, D.A., Pirrotta, V., Hadfield, C., Hall, J.C., and Rosbash, M. 1984. Molecular analysis of the period locus in Drosophila melanogaster and identification of a transcript involved in biological rhythms. Cell 38, 701–710.
[5] Zehring, W.A., Wheeler, D.A., Reddy, P., Konopka, R.J., Kyriacou, C.P., Rosbash, M., and Hall, J.C. 1984. P-element transformation with period locus DNA restores rhythmicity to mutant, arrhythmic Drosophila melanogaster. Cell 39, 369–376.
[6] Siwicki, K.K., Eastman, C., Petersen, G., Rosbash, M., and Hall, J.C. 1988. Antibodies to the period gene product of Drosophila reveal diverse tissue distribution and rhythmic changes in the visual system. Neuron 1, 141–150
[7] Hardin, P.E., Hall, J.C., and Rosbash, M. 1990. Feedback of the Drosophila period gene product on circadian cycling of its messenger RNA levels. Nature 343, 536–540.
[8] Liu, X., Zwiebel, L.J., Hinton, D., Benzer, S., Hall, J.C., and Rosbash, M. 1992. The period gene encodes a predominantly nuclear protein in adult Drosophila. J Neurosci 12, 2735–2744.
[9] Myers, M.P., Wager-Smith, K., Wesley, C.S., Young, M.W., and Sehgal, A. 1995. Positional cloning and sequence analysis of the Drosophila clock gene, timeless. Science 270, 805–808.
[10] Sehgal, A., Rothenfluh-Hilfiker, A., Hunter-Ensor, M., Chen, Y., Myers, M.P., and Young, M.W. 1995. Rhythmic expression of timeless: a basis for promoting circadian cycles in period gene autoregulation. Science 270, 808–810.
[11] Gekakis, N., Saez, L., Delahaye-Brown, A.M., Myers, M.P., Sehgal, A., Young, M.W., and Weitz, C.J. 1995. Isolation of timeless by PER protein interaction: defective interaction between timeless protein and long-period mutant PERL. Science 270, 811–815.
[12] Sehgal, A., Price, J.L., Man, B., and Young, M.W. 1994. Loss of circadian behavioral rhythms and per RNA oscillations in the Drosophila mutant timeless. Science 263, 1603–1606.
[13] Vosshall, L.B., Price, J.L., Sehgal, A., Saez, L., and Young, M.W. 1994. Block in nuclear localization of period protein by a second clock mutation, timeless. Science 263, 1606–1609.
[14] Allada, R., White, N.E., So, W.V., Hall, J.C., and Rosbash, M. 1998. A mutant Drosophila homolog of mammalian Clock disrupts circadian rhythms and transcription of period and timeless. Cell 93, 791–804.
[15] Rutila, J.E., Suri, V., Le, M., So, W.V., Rosbash, M., and Hall, J.C. 1998. CYCLE is a second bHLH-PAS clock protein essential for circadian rhythmicity and transcription of Drosophila period and timeless. Cell 93, 805–814.
[16] King, D.P., Zhao, Y., Sangoram, A.M., Wilsbacher, L.D., Tanaka, M., Antoch, M.P., Steeves, T.D., Vitaterna, M.H., Kornhauser, J.M., Lowrey, P.L., et al. 1997. Positional cloning of the mouse circadian clock gene. Cell 89, 641–653.
[17] Darlington, T.K., Wager-Smith, K., Ceriani, M.F., Staknis, D., Gekakis, N., Steeves, T.D., Weitz, C.J., Takahashi, J.S., and Kay, S.A. 1998. Closing the circadian loop: CLOCK-induced transcription of its own inhibitors per and tim. Science 280, 1599–1603.
[18] Hardin, P.E. 2011. Molecular genetic analysis of circadian timekeeping in Drosophila. Adv. Genet. 74,
141–173.
[19] Price, J.L., Blau, J., Rothenfluh, A., Abodeely, M., Kloss, B., and Young, M.W. 1998. double-time is a
novel Drosophila clock gene that regulates PERIOD protein accumulation. Cell 94, 83–95.
[20] Ceriani, M.F., Darlington, T.K., Staknis, D., Más, P., Petti, A.A., Weitz, C.J., and Kay, S.A. 1999. Lightdependent sequestration of TIMELESS by CRYPTOCHROME. Science 285, 553–556.
[21] Emery, P., So, W.V., Kaneko, M., Hall, J.C., and Rosbash, M. 1998. CRY, a Drosophila clock and lightregulated cryptochrome, is a major contributor to circadian rhythm resetting and photosensitivity. Cell 95, 669–679.
[22] Papazyan, R., Zhang, Y., and Lazar, M.A. 2016. Genetic and epigenomic mechanisms of mammalian
circadian transcription. Nat Struct Mol Biol 23, 1045–1052.
[23] Nohales, M.A., Kay, S.A. 2016. Molecular mechanisms at the core of the plant circadian oscillator.Nat Struct Mol Biol 23, 1061–1069.
[24] Ishiura, M., Kutsuna, S., Aoki, S., Iwasaki, H., Andersson, C.R., Tanabe, A., Golden, S.S., Johnson, C.H., Kondo, T. 1998. Expression of a gene cluster kaiABC as a circadian feedback process in cyanobacteria. Science 281, 1519–1523.
[25] Nakajima, M., Imai, K., Ito, H., Nishiwaki, T., Murayama, Y., Iwasaki, H., Oyama, T., and Kondo, T. 2005. Reconstitution of circadian oscillation of cyanobacterial KaiC phosphorylation in vitro. Science 308, 414–415.
[26] O'Neill, J.S., van Ooijen, G., Dixon, L.E., Troein, C., Corellou, F., Bouget, F.-Y., Reddy, A.B., and Millar,
A.J. 2011. Circadian rhythms persist without transcription in a eukaryote. Nature 469, 554–558.
[27] Ray, S., Reddy, A.B. 2016. Cross-talk between circadian clocks, sleep-wake cycles, and metabolic networks: Dispelling the darkness. Bioessays 38, 394–405.
[28] Balsalobre, A., Damiola, F., and Schibler, U. 1998. A serum shock induces circadian gene expression in mammalian tissue culture cells. Cell 93, 929–937.
[29] Mohawk, J.A., Green, C.B., and Takahashi, J.S. 2012. Central and peripheral circadian clocks in mammals. Annu Rev Neurosci 35, 445–462.
[30] Son, G.H., Chung, S., Choe, H.K., Kim, H.-D., Baik, S.-M., Lee, H., Lee, H.-W., Choi, S., Sun, W., Kim, H., et al. 2008. Adrenal peripheral clock controls the autonomous circadian rhythm of glucocorticoid by causing rhythmic steroid production. Proceedings of the National Academy of Sciences 105, 20970–20975.
[31] Panda, S. 2016. Circadian physiology of metabolism. Science 354, 1008–1015.
[32] Patke, A., Murphy, P.J., Onat, O.E., Krieger, A.C., Özçelik, T., Campbell, S.S., and Young, M.W. 2017. Mutation of the Human Circadian Clock Gene CRY1 in Familial Delayed Sleep Phase Disorder. Cell 169, 203–215.e213.
[33] Toh, K.L., Jones, C.R., He, Y., Eide, E.J., Hinz, W.A., Virshup, D.M., Ptácek, L.J., and Fu, Y.H. 2001. An hPer2 phosphorylation site mutation in familial advanced sleep phase syndrome. Science 291, 1040–1043.
[34] Hirota, T., and Kay, S.A. 2015. Identification of small-molecule modulators of the circadian clock. Meth. Enzymol. 551, 267–282.
[35] Abbott, B. P. et al. 2016. Observation of Gravitational Waves from a Binary Black Hole Merger. Physical Review Letters, vol. 116, 061102.
[36] LIGO Open Science Center (LOSC), https://losc.ligo.org/events/GW150914/
[37] B. Iyer et al. 2011. LIGO-India Technical Report No. LIGOM1100296. https://dcc.ligo.org/LIGOM1100296/public/main
[38] Elmes, J. 2016. Interview with Richard Henderson-The winner of the Copley Medal talks structural biology, fixing cars and sleeping soundly. Times Higher Education.
[39] Dubochet, J. 2016. A Reminiscence about Early Times of Vitreous Water in Electron Cryomicroscopy. Biophys J., 110, 756-757.
[40] Gelfand, A. 2016. The Rise of Cryo–Electron Microscopy. Biomedical Computation Review.






Komentar berhasil disembunyikan.